Sie möchten eine medizinische Studie an bzw. mit Menschen durchführen? Dann müssen Sie Ihr Forschungsvorhaben vorab von einer Ethik-Kommission sowie einer Bundesoberbehörde (PEI/BfArM) prüfen lassen.
Hier erfahren Sie, welche Forschungsvorhaben in Deutschland von einer Ethik-Kommission bewertet werden müssen und nach welchen Kriterien sich die Zuständigkeit einer Ethik-Kommission richtet.
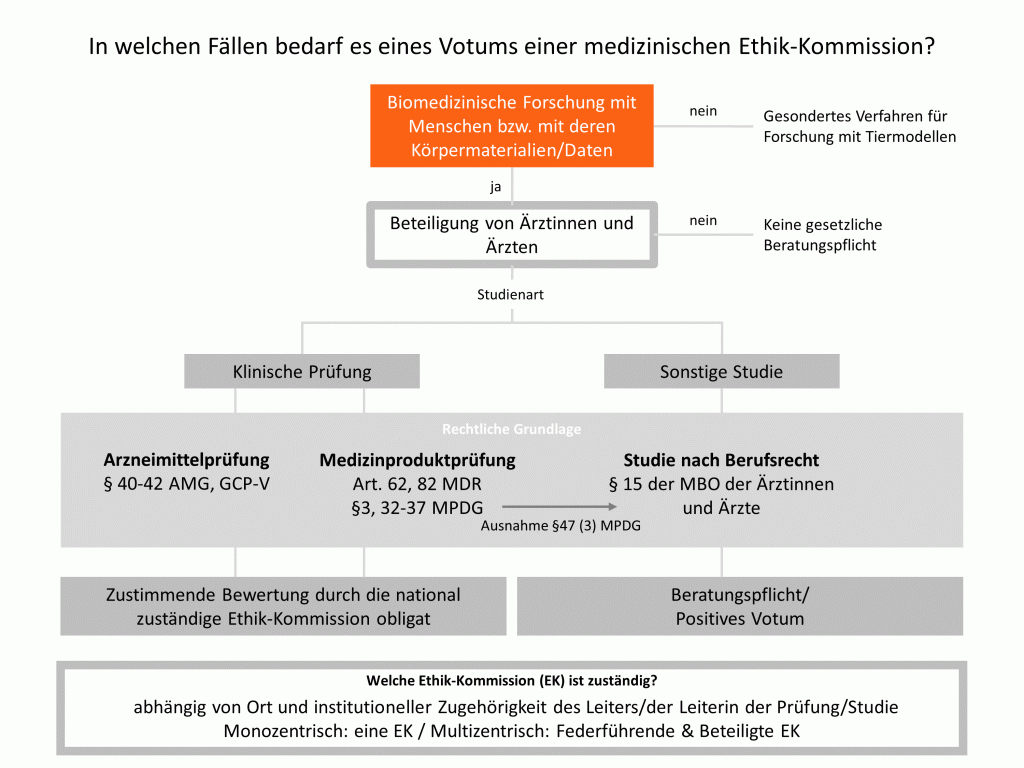
Die Zuständigkeit einer Ethik-Kommission bestimmt sich nach dem Ort des Leiters/der Leiterin der klinischen Prüfung bzw. Studie sowie der institutionellen Zugehörigkeit des Leiters/der Leiterin.
Auf der folgenden Seite finden Sie eine Übersicht der einzelnen medizinischen Ethik-Kommissionen in Deutschland.
Spezialgesetzliche Bestimmungen wie das Arzneimittelgesetz (AMG) und das Medizinproduktedurchführungsgesetz (MPDG) sowie die entsprechenden EU-Verordnungen (CTR 536/2014, MDR 2017/745) regeln die Bewertung von klinischen Prüfungen durch medizinische Ethik-Kommissionen.
Nähere Informationen zur Antragstellung für klinische Prüfungen zu Arzneimitteln und Medizinprodukten finden Sie auf folgenden Seiten:
Als sonstige Studien werden alle medizinischen Forschungsvorhaben mit Menschen bezeichnet, die nicht spezialgesetzlich geregelt sind, an denen jedoch Ärztinnen und Ärzte beteiligt sind. Sonstige Studien unterliegen der Pflicht zur Beratung durch eine Ethik-Kommission gemäß § 15 der Musterberufsordnung (MBO) für Ärztinnen und Ärzte, und zwar in der von den einzelnen Landesärztekammer jeweils verabschiedeten, rechtlich bindenden Fassung.
Auch die Forschung mit Körpermaterialien/ Daten, die sich einem bestimmten Menschen zuordnen lassen, bedarf einer berufsrechtlichen Beratung durch eine Ethik-Kommission Demnach fällt die Errichtung einer forschungsbezogenen Biobank sowie die Nutzung der dort gesammelten Biomaterialen zu Forschungszwecken unter das Antrags- und Beratungsverfahren für sonstige Studien.
Nähre Informationen zur Antragstellung für sonstige Studien finden Sie auf folgenden Seiten:
Nähre Informationen zur Antragstellung, wenn es um Strahlenschutz und Datenschutz geht, finden Sie auf folgenden Seiten: